 |
第七章
细菌和噬菌体的遗传重组 |
| 第一节 基因和基因产物的符号 | |
| 第二节 细菌转化 | |
| 第三节 细菌的接合 | |
| 第四节 高频重组品系 | |
| 第五节 噬菌体染色体的连锁遗传和交换 | |
| 第六节 转导 |
 |
第七章
细菌和噬菌体的遗传重组 |
| 第一节 基因和基因产物的符号 | |
| 第二节 细菌转化 | |
| 第三节 细菌的接合 | |
| 第四节 高频重组品系 | |
| 第五节 噬菌体染色体的连锁遗传和交换 | |
| 第六节 转导 |
基本概念
转化(transformation)是指在生物之间通过细胞外DNA片段的途径来传递遗传物质。经遗传重组转化的DNA分子的一部分能和受体染色体的同源部分置换。转化可以用于确定基因顺序和基因间距离。
转染(transfection)是指用裸露的噬菌体整体DNA转化原核受体细胞的过程。用于真核细胞时,对任何裸露DNA的吸收都称为转染。在酵母和植物中转化和转染的概念是相似的。
接合(conjugation)是通过供体和受体菌细胞间的直接接触能单向转移遗传信息的过程。共体品系的细胞中有一个称为F因子的质粒。接合的结果是将F因子从共体转移到受体中。
转导(transduction)是以噬菌体为媒介将细菌的DNA从共体转移到受体中的过程。转导可以通过小段染色体来进行细菌精细结构作图。
用重组作图的遗传学原理可以用于不同的基因的突变位点之间的距离作图--基因间作图(intergenic mapping)及同一基因内部突变位点的作图--基因内作图(intragenic mapping)。
性导是通过F'因子通过接合将某个特异的基因传递给受体的过程。
转导分为广泛性转导和特异性转导两种。广泛性转导是以P1或P22为媒介,通过"偷渡"和同源重组可将供体的任何基因传递给受体。两个基因间同时被P1转导的现象称为共转导。共转导可用于细菌的精细作图。特异性转导是以λ噬菌体为媒介通过定点整合或重组将特异的基因(gal或bio)传递给受体的过程。
低频转导(LFT)是指通过缺陷型λ(λdg)以较低的频率将gal基因传递给受体。
高频转导(HFT)是指含有λ和λdg的双重溶原菌为供体可将gal基因以很高的频率传递给受体。
研究微生物的重组必定要涉及到基因及其产物、表型和基因型。1983年大肠杆菌的基因位点已有1027个,因此必须要有一个统一稳定的符号才便于描述,1966年Genetics刊登了M.Demerec等建议的大肠杆菌中基因符号的命名系统。1981年Sherman又在此基础上提出了酿酒酵母基因符号的命名规则。现在国际各权威性生命学科杂志也制定了明确的要求,这些要求基本上和以上两大命名系统相一致。综合起来,规定如下:
大肠杆菌和其他细菌:基因座的命名统一用斜体,用三个缩写字母表示;表型第一个字母大写,用正体。基因型三个字母都小写,用斜体。肩上的符号用以表示野生型、突变型、抗性或敏感性,如Gal+表示表型为半乳糖野生型或原养型,Gal-或Gal表示表型为半乳糖突变型或缺陷型;gal+表示基因型为半乳糖野生型,gal-或gal
表示基因型为半乳糖突变型;Amps表示表型为氨基苄青霉素敏感性,ampr表示基因型为氨基苄青霉素抗性,amps表示基因型为氨基苄青霉素敏感性。如一个基因有多个位点时,在基因座名称后用正体的大写字母来表示不同的位点,如LacZ。对于特定的突变型常以它们被分离出来的前后顺序编号来表示,但编号要正写,如galK32。
酵母:三个字母表明基因功能,而后的数字表示不同的基因座。酿酒酵母基因gal4,cdc28;蛋白质GAL4,CDC28。
线虫:用三个小写字母表示突变表型,如存在多个基因座,用连字符后接数字表示。例如,基因unc-86,ced-9;蛋白质UNC-86,CED-9。
果蝇:突变表型的描述可用1~4个字母表示。例如,基因white(w),tailess(tll),hedghog(hh);蛋白质White,Tailess,Hedghog。
植物:虽然没有惯用法适用于所有植物,但大多数用1-3个小写字母表示。Arabidopsis基因用果蝇的方法命名大需要用大写字母。例如,基因AGAMOUS(AG);蛋白质AGAMOUS。
脊椎动物:一般以1-4个小写字母和数字表示其基因功能。例如,基因sey,myc;蛋白质Sey,Myc。
人类:方法如脊椎动物但需大写。例如,MYC、ENO1;蛋白质MYC、ENO1。对于基因产物的命名以前没有统一的规定,现在基本上都统一用正体,或全部大写,或第一个字母大写,如GAL或Gal。
遗传物质在细菌中有三种转移的形式,即转化、接合和转导。这三种转移形式的共同特点是:单方向转移;都产生部分二倍体(partial);基因只有整合到环状染色体上才能稳定的遗传。
转化是通过外源的DNA片段传递遗传信息的过程。此外源DNA片段一般都是人工抽提的,传递时不需要载体,而是利用改变细胞膜的通透性,使外源DNA片段进入细胞,整合到基因组中,改变基因型。在细菌中,转化是非病毒DNA导入细胞的过程。转染是转化的一种特殊形式,用于原核细胞时其外源DNA是特指离体的噬菌体DNA,来感染感受态的细菌,并在其中得到表达。用于真核细胞时,对任何裸露DNA的吸收都称为转染。
细菌转化的现象是在1928年被F.Griffth首先发现的。1944年O.Avery及其同事确定细菌转化因子是DNA。在转化中游离DNA的片段被活的细菌所接受。而导致部分后代遗传性状发生了稳定的改变。转移过程通常用来进行制作细菌的基因图,这种作图方法是接合和转导所不能取代的。在转化作图的实验中,从一个供体品系的细胞中抽提和纯化DNA,然后将它断裂成小的双链片段,再加入到不同基因型的受体细菌的悬浮液中。被受体细胞接受的供体DNA片段就可以和受体染色体的同源部分进行重组,产生重组染色体,由于基因的重组导致了受体表型发生了改变,这个过程就称为转化。在转化中,任何品系都可以作为供体或受体,但供体和受体的基因型应是不同的。
大部分种类的细菌都可以通过转化而重组。但变异的关键在于它们吸收供体DNA的能力。有的细菌如枯草杆菌(Bacillus subtilis)在试管中能很容易被转化,可用这种方法来作图。但野生型E.coli并不容易转化,这是由于细菌产生一种酶能迅速降解进入的外源DNA,经过多年的努力,科学家们发现了一种方法可以增加细胞吸收外源DNA的效率。那就是用化学方法处理细胞,使其改变膜对DNA的通透。这种细胞就称为感受态细胞(competent
cells),即细胞处于能摄取核酸分子时的生理状态。这种方法已经成为基因工程的常规技术,它对于我们利用体外DNA重组技术来了解真核和原核生物的基因功能特别重要。细菌的转化有两种类型:一种是自然转化(natural
transformation),在自然转化中细菌可以自由地吸收DNA,通过它来进行遗传转化;另一种是工程转化(engineered
transformation),在这种转化中,细菌发生改变使得它们能摄入并转化外源DNA。枯草杆菌中的转化就属于自然转化,E.coli转化属于工程转化。
在转化实验中,并非所有的受体细胞都被转化了,实际上只有很少比例的细菌吸收了外源DNA,一旦供体DNA被受体摄取,我们是可以检测到重组的转化产物和受体细胞的染色体。让我们来看一下枯草杆菌转化的例子。
受体染色体上有一个突变基因a,而供体的双链片段上有其野生型等位基因a+;外源DNA双链一条被降解,仅一条被摄入受体细胞;这条单链线状DNA片段和受体的环状染色体的同源部分形成了三链结构;供体的单链DNA和受体双链DNA通过双交换进行重组;结果在双交换区域内,受体染色体发生重组,形成杂合双链a/a
+,带有供体的a+基因,而被取代的单链上却带有受体的等位基因a,后被降解;经复制后产生了两种不同的后代,一种是a+/a+,另一种是a/a,预计各站2一半。贵恙于高度感受态的受体细胞用过量的外源DNA片段进行转化,转化的频率约为10-3,即103个细胞中约有一个被转化。
通过转化可以测定基因的连锁、基因的排列顺序以及图距。原理如下:如果在供体的染色体上有两个离得很远的基因a+和b+,我们将会发现它们总是在不同的DNA片段上,这样如果有一个a+b+供体和ab受体,那共转化(contransformation)即两个基因同时转化的概率是两个基因单独转化概率的乘积。若每个基因的转化产生率是10-3
的话,那么这两个基因被同时转化的频率是10-6 。如果两个基因离得很近,有可能位于同一个DNA片段上,那么它们共转化的频率将接近单个基因转化的频率。我们也可以这样说,若共转化的频率要比两个单个基因转化频率乘积高的话。那么这两个基因一定大紧密连锁的。
基因的顺序也可以通过共转化的结果来分析确定。,p+和q+常常共转化,而q+和o+也常常共转化,但基因p+和o+从未发生共转化,那么这三个基因的顺序一定是pqo。
由于遗传学家可以控制转化片段大小,因此两个基因共转化的频率可以和转化片段的平均大小相等。通过转化片段平均大小相关的共转化频率测定,就可以获得这些基因的连锁图谱。
一、E.coli接合的发现
1946年莱德伯格(J.Lederberg)和塔特姆(Tatum)发现在细菌之间转移遗传物质的另一种方法――接合。细菌接合是指通过细胞的直接接触,遗传信息从供体单向转移到受体的过程。
在Lederberg发现这种方法以前,人们已经对细菌的杂交进行了探索,但存在两大难题不易解决。1.a+b-× a-b+-----杂交后得到重组子(a+b+)的频率很低,和基因回复突变频率相近,难以区别。也就是说难以确定a+b+是由两个亲本回复突变产生还是真正的重组子。2.
E.coli杂交产生重组频率为10-7 ,也就是说要检查千万个菌落才能发现一个重组菌落,工作量太大。 Lederberg采用了两个措施便巧妙地解决了这两个难题。一是使用多重突变型(multiple
auxotroph)品系作为亲本进行杂交,由于两个或多个基因在同一亲本中同时发生回复突变的频率很小很小,这样可一十分信服地将重组子和回复突变区分开。二是采用了以基本培养基来筛选原养型的方法。由于制备多重突变型亲本工作量很大,正好在此不久前斯坦福大学的Tatun分离出了各种E.coli的生化突变型,于是Lederberg遍邀请了这位曾和比德尔合作建立"一基因一酶"学说的微生物专家合作。巧的是Tatum就在E.coliK12品系中挑选了多重突变型,而正好K12中是有F因子的,这是事前并不知道的,只不过K12是他在教学工作中多年使用的品系。如果当时要是采用了不含F因子的品系,那么实验那难以成功,至少接合的发现要延迟数年。因此他们的这次合作在科学史上是一桩幸运的事,由于他们的特殊贡献,1958年Beadlr,Tatum和Lederberg获得诺贝尔奖。
他们选用两个E.coliK12多重突变品系:A品系:met- bio- thi+ leu+ thr+ ;B品系:met+ bio+ thi- leu-
thr- 。将它们分别接种在基本培养基上都不能生长。若将它们混合后离心洗涤,除去完全培养基,再制成悬液以对照组相同的浓度接种于基本培养基,结果获得了野生型。其出现的频率是10-7。E.coli许多生化突变型回复突变的频率是10-7,假如由亲本A两个位点同时回复突变形成野生型,其概率应该是0-14;若B品系三个位点同时回复突变,其概率是10-21,与重组子出现的频率相差很大,故可以排除回复突变的可能性。
虽然回复突变的可能排除了,但人们仍提出以下质疑;1.细菌杂交实验获得的重组子可能是转化的亿个微度 。因为有可能一种亲本的细胞在处理过程中发生破裂释放出转化因子,和另一亲本重组而产生部分的原养型。2.培养基中含有某些代谢产物,混合后这些产物互相补充了对方的足而得以在基本培养基上生长。这两个问题是尖锐而深入的。为澄清这个问题,莱德伯格和塔特姆将一种亲本的培养基经过细菌漏斗过滤,除去细胞,然后再加入另一亲本的培养物中,结果未产生原养型。如果杂交实验中可以产生转化因子
即DNA片段或某些可以互相补充的产物,那么它们是可以通过过滤器进入滤液中,进一步和受体作用,产生原养型,但结果正相反,说明也可以排除以上质疑,并提示A和B品系细菌的直接接触似乎是出现原养型的必要条件。1950年戴维斯(B.D.Davis)设计了U形管实验,进一步支持了上述结论。U形管的底部有一砂芯横隔,上有微孔,可以通过0.1μm以下的颗粒,细胞无法通过。戴维斯将A、B品系分别放入U形管的两侧,一侧塞上棉塞,另一端接上注射器。当两种细菌培养物都增生到饱和状态时,用注射器轻轻地把培养液从一臂经过滤器吸到另一臂。再轻轻地压过去,让培养液充分混匀,但两种品系的细胞无法接触,然后两侧的A、B菌株离心洗涤后涂布到基本培养基上,都不出现菌落,即不产生重组子。若培养液中有转化因子DNA,或代谢产物的话是可以在两个品系之间充分交流的,但并未引起重组,因此完全可以排除转化和代谢产物互相补充的可能性,而清楚的表明,两个亲本的细胞不互相接触是不能进行杂交的,这为研究接合的本质奠定了基础。由于历史的局限,从一开始莱德伯格和塔特姆就根据真核的重组来解释他们的发现,认为细菌接合是一个彼此交换遗传物质的过程,即细菌同宗配合(homothalic)。导致1951年莱德伯格根据自己的实验,将E.coli的连锁图绘成三叉戟状,使E.coli连锁图的绘制陷入困境。任何一个伟大的科学家在他整个的一生中难免会出现一些失误,但他们那种创新的精神,求实的态度永远值得后人学习和赞美。
三种不同的致育因子的相互关系
现在把雄性菌株(male Strains)的不同致育因子F’,Hfr,F的关系概述如下。
(1)F’是带有部分细菌染色体的F因子,它的性质在F和Hfr之间。Hfr通过交换,可以形成带有部分细菌染色体的 F’因子,而 F’因子又可通过交换整合到细菌染色体上的原来位置,回复到以前的Hfr状态。
(2)F’因子连同它所带有的部分细菌染色体可一起移到F-细胞,其转移速率近于F因子。利用F’可以形成部分二倍体,进行重组研究。F’因子偶而也可把它所在的供体细菌的染色体转移到
F-细胞,这是由于 F’的整合,所以供体细菌染色体上基因的转移方向和顺序跟 F’所来自的Hfr一样。
(3)有F因子的细胞是F+细胞,没有F因子的细胞是F-细胞。相对于每一细菌染色体,有 1―3个F因子,F因子的复制是自律的。F+×F-,F因子由供体进入
F-细胞,使受体细胞成为F+细胞,但供体细胞仍为F+,其染色体很少转移。F因子可通过简单交换整合到细菌染色体上,形成 Hfr染色体。反过来,通过简单交换,又可从Hfr染色体产生F因子。不同的Hfr菌株的染色体转移起始点和方向不同,这是由于F因子整合的位置和方向不同的缘故。
(4)Hfr能以高频率反民细菌染色体转移到F-细菌中,而F因子因位于Hfr染色体的最末端,极少进入。F’因子和F因子很容易转移到F-细胞中,但供体染色体的转移率很低。
一.烈性噬菌体
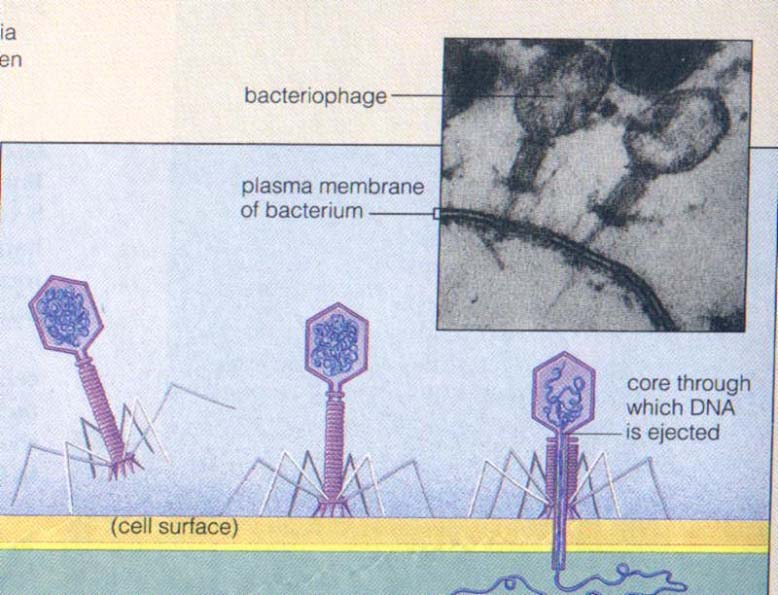
烈性噬菌体(virulent phage)是使宿主菌发生裂解的噬菌体。它在侵染细菌时,先吸附到菌体表面的特异受体上
,由噬菌体所产生酶的作用下,在细菌细胞壁上形成一个微孔,把它的头部中所含的核酸――遗传物质――注入到菌体内。噬菌体核酸所带的遗传信息把宿主菌的生物合成装置接收过来。停止合成细菌成分,使细菌的合成装置转为合成更多的噬菌体成份,最后细菌细有包裂解(lysis),释放出很多子代噬菌体。
研究噬菌体的方法:多采用研究噬菌斑的方法。噬菌斑是一个噬菌体裂解一个细菌后,子代噬菌体感染邻近的细菌,这些细菌又裂解,再侵染其它细菌,最后形成的一个圆形的透明区。噬菌斑的形态(plaque
morphology),包括噬菌斑的大或小,边缘清晰或模糊等等。另一些遗传上可以分析的噬菌体性状是宿主范围(host range),某些细菌菌株不受噬菌体的吸附,而噬菌体能感染和裂解的细菌菌株也可以不同。
二.噬菌体的基因重组
从野生型噬菌体可以分离出突变型。各突变型的性质可以传给后裔。用两种突变型噬菌体感染同一宿主茵,它们的后裔可以出现重组子。在40年代早期,Dethrdck就注意到了噬菌体的这些性质,进行了遗传学分析。
现在来看烈性的两对性状及其重组。
T2噬菌体 菌斑的大小(直径) 周边 透明度(与寄主范围有关)
野生型r+ 1mm 模糊 h+,半透明(侵染菌株B,不能侵染菌株 B/2)
突变型r 2mm 清晰 h,透明(侵染菌株B和B/2)
进行重组实验时,把上述两个亲本噬菌体(hr+和h+r)去感染菌株B,噬菌体的浓度要高 ,使有高比例的细菌同时受到两种噬菌体的感染(称为混合感染或复感染,mixed
or double infection)。 把释放出来的噬菌体(子代噬菌体)接种在同时长有菌株B和B/2的培养基上。得到4种噬菌斑,透明而小(hr+)和半透明而大(h+r)是亲组合,半透明而小(h+r+)和透明而大(hr)是重组合。计算重组值。不同的快速溶菌突变型在表型上不同,记作ra,
rb, rc等。用不同快速溶菌突变型(rxh+)与宿主范围突变型(r+h)杂交, 得出结果,作一加锁图。
只 有当很多不同的T2品系发现后,进行广泛的遗传学作图,我们才发现原来T2噬菌体的连锁图也是环状的。事实上,T2连锁群的图距总长约1500图距单位(map
unit)
(2)特异性转导 我们现在介绍另一类噬菌体,它们所进行的转导是特异性转导(specialized
transduction), 或局限性转导(restricted transduction),这类噬菌体只转移细菌染色体的特定部分。
上面讲到过的λ噬菌体是特异转导者(transducer)的一个很好例子。大肠杆菌的一个溶源菌株 K12(λ)可由紫外光诱导,用来进行转导。唯一成功的转导包括gal座位。根据实验知道,λ总是附着到gal座位的邻近位置。转导过程中有一些值得注意的特点:(1)所有gal+转导子(transductants)对λ噬菌体的超数感染(superinfection)都是免疫的,但gal+转导子在菌体裂解时不能产生成熟的λ噬菌体,可见带有gal+的人噬菌体是有缺陷的,记作λd
gal+(λ-defective gal+)。(2)λdgal+转导粒子(transducing particles)约丧失 25%的噬菌体染色体,但具有完整的λ外壳,所以仍能感染细菌。(3)以λdgal+转导粒子去感染
gal―细菌,所形成的gal+转导子中有相当一部分是不稳定的,能持续地产生gal―分离子(segregants),所以这些不稳定转导子是部分一倍体,除了受体染色体上的gal―外,还有
λd原噬菌体上的 gal+,基因型应为λd gal+/ga1―。
三.溶源性细菌
这一类噬菌体感染细菌后,除偶而情况外,不出现溶菌现象,称为温和噬菌体(temperate phage)。温和噬菌体感染细菌后,可采取两种增殖周期中的一种:其中一种是溶菌周期,细菌受到感染后,菌体内噬菌体迅即增殖,菌体被裂解,噬菌体释放出来。这一周期是偶而自发产生的,也是烈性噬菌体所必然采取的。另一种是所谓溶源周期,细菌受噬菌体感染后,好象未被感染一样,细菌继续增殖。这时受感染的细菌具有下列两个特征:
(1)细菌细胞内已有侵入的噬菌体,再也不会受到同一种噬菌休的侵染,也就是说,有了免疫性。这种免疫性的特程度很高。
(2) 这种细菌即使没有外来噬菌体的感染,有时偶而也会自发地释放噬菌体。如进行诱导(induction),则能一齐地释放成熟噬菌体。有些细菌带有某种噬菌体,但并不立即导致溶菌,这种现象称为溶源性(lysogeny),而这样的细菌秒为溶源性细菌或溶源菌(lysogenic
bacteria)。受温和噬菌体感染的细菌,几乎都成为溶源菌,而且能把这种特性传给子代细胞。从单个溶源菌开始的培养中。所有的细菌都是溶源菌,只要不进行诱导,溶源性几乎可以半永久性地传下去。
溶源性的遗传基础 将细菌细胞内含有无感染能力的噬菌体称为原噬菌体(prophage)。溶源菌中原噬菌体的存在形式有两种:一种是染色体外的以游离形式存在,另一种是整合到细菌染色体上。原噬菌体在细菌细胞中采取哪一种形式,噬菌体的种类而定。P1以游离状态存在,而λ以及φε0,μ等以整合状态存在。F+与F-细胞间进行杂交,发现杂交结果与所用的溶源菌菌株有关。如
F+×F-(λ),即F-细胞是带有λ噬菌体的溶源菌时,可偶而产生溶源性重组子;而反交F+(λ)×F-,即 F+细胞是带有λ噬菌体的溶源菌时,几乎不产生溶源性重组子。
当Hfr菌株被用于遗传学分析以后,这些结果就容易理解了。在杂交 Hfr×F-(λ)中,Hfr基因转移到 F-细胞,所以有 Hfr基因的溶源性F-重组子很容易得到。然而在反交Hfr
中,Hfr菌株的前端基因可在F-受体中出现,但后端基因的重组子得不到。因为溶源性H好跟非溶源性F-受体杂交时,经过一定时间,λ原噬菌体进入一个无免疫能力的细胞,原噬菌体随即开始复制,使细胞裂解,释放出游离的噬菌体,这个现象叫做合子诱导(zygotic
induction)。既然原噬菌体进人非溶源性细胞后,使受体细胞裂解,这样在λ噬菌体转移以后才进人 F-细胞的Hfr后端基因就无法得到了。上面谈到的 F+(λ)×F-,几乎不出现溶源性重组子,就是因为λ进入F-细胞后,使F-细胞裂解,所以就得不到溶源性重组子了。
通过中断杂交试验可以证明,λ原噬菌体在一特定时间进入F-细胞,这时间跟gal(半乳糖发酵基因)的进人时间密切有关,表示λ原噬菌体所在的地点就在gal座位的附近。
二、单向转移和F因子
1952年海斯9W.Hayes)的意外发现动摇了"细菌同宗配合"观点,使细胞接合的研究又转向正确的方向。
海斯在重复莱德伯格和塔特姆的细菌杂交实验之前,分别用高剂量的链霉素来处理A品系和B品系,结果A品系受处理后,杂交结果不受影响,而B品系受处理后完全阻止了重组的发生。这对海斯来说意味着两个品系在杂交过程中的作用是不同的,也就是说可能不是交互的过程,而是一个单向的过程。因为链霉素可以阻止细胞分裂继而杀死细胞。大它还允许交配持续一个短时间。A品系在交配后被杀死并不影响杂交结果,表明它是一种供体,像雄性动物一样,交配后被杀死,不会影响后代。海斯的结论认为细菌的接合是异宗配合(heterothalic)过程,两个亲本在杂交中所起的作用不同,有供体和受体之分,相当于雄性和雌性。
以上结论得出后不久,海斯将放在冰箱中有一年之久的一个菌种A(str-s)雄和B(str-s)雌杂交,结果和预期的不同,不能产生重组子,海斯对这一偶然得以外情况并没有掉以轻心,而是继续实验和分析。他将此菌进行诱变,使str-s变成str-r,以便和A(str-s)杂交,结果是可育的产生了A(str-r),在进一步和B(str-s)杂交,结果是可育的。说明原来是"雄"性的A品系放在冰箱中一年,变成了雌性,即从供体变成了受体。以上实验完成后不久,莱德伯格和他的妻子E.Lederberg以及L.L.Cavalli也发现了这一现象,他们对此一致的解释是:所谓的供体或雄性是细菌的细胞内有一种致育因子(fertility,F),以F+表示,而雌性品系是缺乏这种F因子,以F-表示。原来的雄性品系是F+放置在冰箱中一年后丢失F因子,变成了F-,作为F-的A品系是不能和另F-的B品系杂交的,所以不育。经诱变后其基因型由(str-s)变成了)str-r),但仍然是F-,故可以和F+的A品系(str-s)杂交,经str选择培养基筛选出重组子仍是F+,和F-(str-s)杂交仍然可育,这样便发现了F因子。
F因子是一种质粒,由共价环状闭合DNA双链构成,全长94.5kb,主要分为三个区域:1.重组区;2.自主复制区;3.转移区。重组区中有4个插入顺序(insertion
sequence,IS),通过和宿主染色体上的IS同源重组或通过转座(transpositon)F因子可以整合到宿主不同位点上。由于宿主染色体上IS方向不同,所以整合的方向也随之不同。自主复制区有转移的起点和2个复制起始点,复制起点oriT是在染色体转移时进行滚环复制时的复制起点,oriV是在营养时期,即游离在细胞质中独立复制时的复制起点。转移区主要有合成性伞毛即F纤毛(Fpill)的操纵子。F纤毛是由性伞毛蛋白构成,呈管状,又叫接合管。通过接合管可将供体和受体细胞相联。1957年拍到第一张接合照片。当时对F因子知道得并不透彻,也不知道重组体是怎样产生的,但从各种实验的结果推论出以下结论:有F因子的细菌称为F+,细菌繁殖时可把F因子传递给后代;没有F因子的细菌称为F-,F+细菌经过丫啶橙处理而丢失,成为F-。F因子一经丢失,细胞中变不在出现;F+可以和F-杂交,而不能和F+杂交;F+和F-的杂交后代皆为F+,而且可以10-7频率获得重组后代。F因子介导的接合也和滚环复制有关。其转移区(transfer region)长33kb。此是接合所需要的。这一段含有40个基因和DNA转移有关(整个基因组约有60个基因),其中主要的基因及功能见表8-3。这些基因叫tra,它们主要的部分作为一个32kb的转录
单位(traY-1)协同表达。TraM和traJ分开表达(图8-8)。traJ是调节traM和traY-1两者的打开,在另一条链上的finP是一个调节子,产生一个小分子反义RNA,关闭traJ。它的激活需要另一些基因finO的表达。转录单位中的某些基因直接和DNA的转转移有关,但大多和细胞的特点有关。
细菌表面的性伞毛巾(pilli)是由F因子编码的。traA编码了伞毛蛋白(pillin)的单个亚基,由此聚合为伞毛。至少有12个tra 基因是修饰和聚合伞毛蛋白的,为伞毛所必需。F性伞毛为毛发状结构,长2-3um,由细胞表面伸出,一个典型的F+细胞有2-3根性伞毛。这些伞毛蛋白亚基聚合成中空的管子,直径8nm,中间有2nm的轴孔。并不是遗传物质转移的孔道。供体细胞不会接触其他F+细胞,那是因为traS和traT编码了表面排斥蛋白,这种蛋白使细胞有效地限制了F+和F+细胞接合。F性伞毛还可以提供RNA噬菌体和某些单链DNA噬菌体,如M52、R17、f1等吸附位点。因此F+细菌对这些噬菌体是敏感的,而F-细菌是抗性的。在供体细胞和受体细胞
开始接触时是易断裂的,但另外一些tra基因起到稳定联接的作用,使接合的细胞紧密联接在一起。性伞毛对起始配对是必要的,但一旦起始以后即性伞毛收缩和消失,结合的细胞已彼此紧密接触了。DNA转移时必须有一个通道通过。但性伞毛并不存在这种通道。因此这种通道仍未确认出来。但traD可能提供了通道或通道的一部分。